"Серебришко"
Платина в перекладі з іспанскої буквально означає «серебришко». Пояснюється така зневажлива назва, дана цьому металу конкістадорами, виключно тугоплавкістю платини, яка не піддавалася переплавці, довгий час не знаходила застосування і коштувала вдвічі нижче, ніж срібло. Зараз на світових біржах платина дорожче срібла приблизно в 100 разів.
_______________________________________________________________________________________________________________________________
Невидимі чорнила
Хлорид кобальту можна успішно використовувати для тайнопису : літери , написані його розчином, що містить в 25 мл води 1 г солі , абсолютно невидимі і проявляються, роблячись синіми, при легкому нагріванні паперу.
_______________________________________________________________________________________________________________________________
Правда і дійсність любові
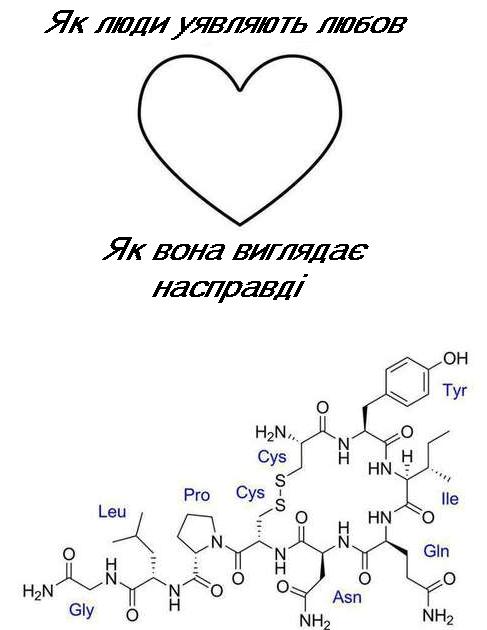
__________________________________________________________________________________________________________________________________
Танцюючий кальмар
Неймовірно, але факт: по-особливому приготований кальмар може станцювати шалену сальсу прямісінько в тебе на тарілці. Танцюючий кальмар -один з вишуканих кулінарних шедеврів японської кухні. Нещодавно вбитого молюска кладуть на тарілку з відвареним рисом і щедро поливають соєвим соусом. Тільки уяви собі, щупальця кальмара починають ворушитися! В чому ж секрет?
Виявляється, нервові волокна кальмара влаштовані так, що навіть після смерті реагують на йони Натрію, що входить до складу соусу, змушуючи м`язи скорочуватись. Ось така хімія :)
__________________________________________________________________________________________________________________________________
Які птахи допомагали шахтарям?
Канарки дуже чутливі до вмісту в повітрі метану. Цю особливість використовували в свій час шахтарі, які, спускаючись під землю, брали з собою клітку з канаркою. Якщо співу давно не було чути, значить слід було підніматися наверх якнайшвидше.
__________________________________________________________________________________________________________________________________
Чому водоспад у Антарктиді червоний?
В Антарктиді з льодовика Тейлора часом виходить Кривавий водоспад. Вода в ньому містить двовалентне залізо, яке, з'єднуючись з атмосферним повітрям, окислюється і утворює іржу. Це і додає водоспаду криваво-рудий колір. Однак двовалентне залізо у воді виникає не просто так - його виробляють бактерії, що живуть в ізольованій від зовнішнього світу водоймі глибоко під льодом. Ці бактерії зуміли організувати життєвий цикл при повній відсутності сонячного світла і кисню. Вони переробляють залишки органіки, а «дихають» тривалентним залізом з навколишніх порід.
__________________________________________________________________________________________________________________________________
Як винайшли непробивне скло
У 1903 році французький хімік Едуард Бенедиктус ненавмисно впустив колбу, заповнену нітроцелюлозою . Скло тріснуло, але не розлетілося на дрібні шматочки. Зрозумівши, в чому справа, Бенедиктус виготовив перші лобові стекла сучасного типу, щоб зменшити кількість жертв автомобільних аварій.
__________________________________________________________________________________________________________________________________
Цікава властивість срібла
IV столітті до нашої ери війська Олександра Македонського вторглися до Індії. На берегах річки Інд у військах вибухнула епідемія шлунково-кишкових захворювань, яка, як не дивно , не торкнулася жодного воєначальника. Виявилося , що прості воїни користувалися олов’яним посудом, а їх командири — срібним. Тоді й згадали, що перський цар Кір II Великий про час військових походів наказував зберігати питну воду в срібних посудинах . Багато пізніше римські легіонери стали носити панцири, наколінники і поножі зі срібла. Срібло має бактерицидні властивості, тому сприяло швидкому загоєнню ран без нагноєнь
__________________________________________________________________________________________________________________________________
Метали
Якщо ви думали , що залізо — міцне і надійне, ви помиляєтеся. Залізо, нагріте до 5000 градусів Цельсія, стає газоподібним.
Безліч хімічних елементів отримали свою назву на честь країн або інших географічних об’єктів. Відразу 4 елемента — Ітрій , Ітербій , Тербий і Ербій — були названі на честь шведського села Іттербю, біля якого виявили велике родовище рідкоземельних металів.
За легендою, думка про систему хімічних елементів прийшла до Менделєєва уві сні, проте відомо, що одного разу на запитання, як він відкрив періодичну систему, вчений відповів: «Я над нею, може бути, двадцять років думав, а ви думаєте: сидів і раптом … готово».
Літій — найлегший метал. Він спливає, наприклад, в гасі.
__________________________________________________________________________________________________________________________________
Цікаві факти з хімії, які ви точно не знали:
Наприклад, коли ми ріжемо цибулю і «плачемо» – то заслуга цих фіктивних емоцій належить саме сірці, яка вбирається в грунт, де росте цибуля. У провінції Індонезії існує вулкан, повністю заповнений сіркою, який носить назву Кава Иджен. Вона осідає на трубах, після чого робочі збивають її арматурою і несуть на зважування. Там таким чином вони заробляють собі на життя. Гігієнічні «продукти» на основі сірки створені спеціально для чистки проблемної шкіри від вугрів і висипки. Вушна сірка, яку нас привчили видаляти ще з дитинства ватними тампонами, «отруює» наше життя з благородними намірами. У ній містяться особливі ферменти лізозіма; саме вони «не пускають» в наш організм бактерії.
__________________________________________________________________________________________________________________________________
Гідрогель для зрощування переломів, заслужений винахід в хімічній промисловості
Гідрогель для зрощування переломів, заслужений винахід в хімічній промисловості. Біоінженери з Університету Райса створили гідрогель, який миттєво переходить з рідкого стану в напівтвердий при температурі, близькії до температури тіла людини, а потіпоступово руйнується. Гель може застосовуватися в якості підтримки для зламаних кісток або інших тканин в організмі пацієнта. При кімнатній температурі гідрогель залишається рідким, але при попаданні в тіло пацієнта він твердне і заповнює вільний простір, який пізніше заросте природною тканиною. Також гідрогель може застосовуватися для доставки стовбурових клітин до скелетних дефектів, що має викликати прискорену регенерацію кісткової тканини. Після виконання своїх функцій гель розкладається і виводиться з організму. Автори відкриття очікують, що гель можна буде налаштувати таким чином, щоб швидкість його розкладання відповідала різним темпам росту кістки.
__________________________________________________________________________________________________________________________________
У якому випадку етиловий спирт може служити протиотрутою?
Метиловий спирт за смаком і запахом не відрізняється від етилового, проте його дія на організм є набагато загрозливішою для нашого здоров’я. Навіть невелика кількість метанолу може призвести до сліпоти, а доза від 30 мл — до смерті. Цим пояснюються часті випадки отруєння метиловим спиртом або через незнання, або в разі вживання підробленого алкоголю. Цікаво те, що у разі такого отруєння протиотрутою є звичайний, тобто етиловий спирт. Це пов’язано з тим, що процеси зв’язування обох спиртів в організмі відбуваються за участю одного ферменту — алкогольдегідрогенази, але так як реакція з етанолом відбувається швидше, шкідливих продуктів розщеплення метанолу в крові в результаті виявляється набагато менше.
__________________________________________________________________________________________________________________________________
Алюміній
У 1827р. видатний німецький лікар і хімік Фрідріх Велер отримав раніше незнаний метал: він нагрівав алюміній хлорид – відому вже сіль – з калієм. У результаті отримав сірий порошок, який при розтиранні ставав зовсім блискучим. Але отримати з цього порошку злиток ніяк не вдавалось. Лише в 1845р. це вдалося Велеру – він отримав крупинку металу величиною з головку від голки. Тоді було велике здивування, бо цей метал, подібний до срібла, був учетверо легший за нього, і втричі - від заліза. Оскільки цей метал був отримати з галунів (по-латині «алюмен») то й назвали метал алюміній. Спочатку метал цінувався дорожче від золота і йшов лише на прикраси. Цікаво, що імператор Франції Наполеон III хотів одягти своїх солдатів в алюмінієві доспіхи , але метал був надто дорогим. Так що їх отримала тільки особиста охорона імператора.
Тільки в 1886р. американський студент Чарльз Хопп і французький інженер П`эр Еру розробили способ виділення Аl електролізом глинозему, розчиненого в розтопленому кріоліті. Але й кріоліт був дефіцитом, тому Аl залишався дефіцитним металом, поки в 1900р. не був розроблений синтетичний спосіб отримання кріоліту.
__________________________________________________________________________________________________________________________________
Про сіре олово
Морозною зимою 1916р. партія олова була відправлена по залізниці з Далекого Сходу в європейську частину Росії. Але на місце прибули не сріблясто-білі зливки, а переважно дрібний сірий порошок.
За чотири роки до цього відбулася катастрофа з експедицією полярного дослідника Роберта Скотта. Експедиція, що направлялася до Південного полюса, залишилася без палива: воно витекло з залізних судин крізь шви, пропаяні оловом.
Приблизно в ті ж роки до відомого російського хіміка В.В. Марковникова звернулися з проханням пояснити, що відбувається з лудженими чайниками, якими постачали російську армію. Чайник, що принесли в лабораторію , як наочний приклад, був покритий сірими плямами і наростами, що обсипалися навіть при легкому постукуванні рукою. Аналіз показав, що і пил, і нарости складалися тільки з олова, без будь-яких домішок.
__________________________________________________________________________________________________________________________________
Олово
Вперше інтерес до оловоорганіки виник у роки першої світової війни. Майже всі органічні сполуки олова, отримані на той час, були токсичні. Як отруйні речовини ці сполуки не були використані, їх токсичністю для комах, цвілевих грибків, шкідливих мікробів скористалися пізніше. На основі ацетату трифенілолова (С6Н5) 3SnOOCCH3 був створений ефективний препарат для боротьби з грибковими захворюваннями картоплі та цукрового буряка. У цього препарату виявилася ще одна корисна властивість: він стимулював ріст і розвиток рослин.
Для боротьби з грибками, що розвиваються в апаратах целюлозно-паперової промисловості, застосовують іншу речовину – гідроокистрибутилолову кислоту (C4H9) 3SnOH. Це набагато підвищує продуктивність апаратури. Його використовують у ветеринарній практиці як засіб проти гельмінтів.
На основі оловоорганічних сполук створені ефективні інсектициди; олово органічне скло надійно захищає від рентгенівського опромінення, полімерними свинець - та олово органічними фарбами покривають підводні частини кораблів, щоб на них не наростали молюски.
________________________________________________________________________________________________________________
Йод
Йод відкрив в 1811 році французький хімік Б. Куртуа. Винуватцем відкриття був улюблений кіт Куртуа: він лежав на плечі хіміка, коли той працював в лабораторії. Бажаючи розважитися, кіт стрибнув на стіл і зіштовхнув на підлогу судини, які стояли поруч. В одній з них перебував спиртовий розчин золи морських водоростей, а в іншій – сірчана кислота. Після змішання рідин з’явилася хмара синьо-фіолетового пару, що було не чим іншим як йодом.
________________________________________________________________________________________________________________
Сірка і цибуля
Коли ми ріжемо цибулю і «плачемо» – то заслуга цих фіктивних емоцій належить саме сірці, яка вбирається в грунт, де росте цибуля.
________________________________________________________________________________________________________________
Хімія мозку
У головному мозку людини за одну секунду відбувається 100 000 хімічних реакцій.
________________________________________________________________________________________________________________
Новий хімічний елемент отримав ім'я Коперніка
Німецькі вчені нарешті вигадали назву новому хімічному елементу, відкритому ще 13 років тому.
Найбільш важкий елемент періодичної системи Менделєєва під номером 112, відкритий (синтезований) в 1996 році, нарешті отримав власну назву.
Група вчених з Інституту дослідженню важких іонів імені Гельмгольца запропонували назвати його "копернікієм", на честь польського астронома Миколи Коперніка, який створив в XVI столітті геліоцентричну картину світу.
"Ми хотіли б вшанувати пам'ять видатного ученого, який змінив точку зору людини на світ", - зазначив Сігурд Хофман, голова наукової групи, яка відкрила елемент.
Зараз "копернікій" є найважчим з офіційно підтверджених атомів. Затримка з визначенням назви у 13 років була пов'язана з необхідними процедурами в Міжнародному союзі чистої і прикладної хімії. Досі його робочою назвою було "унунбій" (від латинських цифр "один-один-два").
112-й елемент також пропонувалося назвати "віксхаузій", "гельмгольцій", "венусій", "штрассманій" і "гейзенбергій". Науковому співтовариству дається півроку на обговорення назви, після чого Міжнародний союз теоретичної і прикладної хімії закріпить обране ім'я за даним елементом.
_____________________________________________________________________________________________________________
Рекорд с відкриття хімічних елементів
Найбільшу кількість хімічних елементів (9) відкрив (синтезував) видатний американський учений Г. Сіборг разом зі своїми співробітниками: в 1940 р. – плутоній, у 1944-1946 рр. – америцій і кюрій, у 1949-1950 – берклій, каліфорній, у 1952-1954 – ейнштейній, фермій, у 1955 – менделєвій, у 1958 р. – резерфордій (нобелій).
________________________________________________________________________________________________________________
Озон
У природі озон утворюється з молекулярного кисню під дією ультрафіолетових променів у стратосфері на висоті 15-30 км над рівнем океану. Озоновий шар дуже розріджений і якби його вдалося стиснути при звичайному атмосферному тиску, він мав би товщину всього 2-3 мм! Незважаючи на це, озон – надійний щит від палючих і смертоносних короткохвильових ультрафіолетових променів. Молекули озону збирають ультрафіолетові промені...
У нижніх шарах атмосфери утворення незначних кількостей озону спричинюється блискавками, чим і пояснюється відчуття свіжості в повітрі після грози.
________________________________________________________________________________________________________________
Низка хімічних фактів
________________________________________________________________________________________________________________________________________________________________
Почему вода хранит много тайн?
В старой доброй формуле H2O, казалось бы, не заключено никаких тайн. Но на самом деле вода – источник жизни и самая известная жидкость в мире – таит в себе множество загадок, неподвластных даже ученым. Пять самых известных «странностей» воды – перед вами.
1. Горячая вода замерзает быстрее холодной.
Возьмем две емкости с водой: в один нальем горячую, а в другой — холодную воду. Поместим их в морозильную камеру. Емкость с горячей водой замерзнет быстрее, чем с холодной, хотя по логике вещей, первой должна была превратиться в лед емкость с холодной водой: ведь горячей надо сначала остыть до температуры холодной, а потом уже превращаться в лед, а холодной остывать не надо. Почему же так происходит?
В 1963 году ученик старших классов Эрасто Б. Мпемба заметил, что горячая смесь застывает в морозильной камере быстрее, чем холодная. Учитель физики, с которым юноша поделился открытием, поднял его на смех. К счастью, ученик оказался настырным и убедил учителя провести эксперимент, который и подтвердил его правоту. Теперь феномен горячей воды, замерзающей быстрее холодной, носит название «эффект Мпемба». Ученые так до конца и не понимают природу этого явления, объясняя его разницей в переохлаждении, испарении, формировании льда и т.д.
2. «Сверхохлаждение» предотвращает формирование льда.
Все знают, что вода всегда превращается в лед при охлаждении ее до нуля градусов по Цельсию… за исключением тех случаев, когда этого не происходит! «Сверхохлаждение» – это склонность воды оставаться жидкой, даже будучи охлажденной до температуры ниже точки замерзания. Это явление становится возможным благодаря тому, что окружающая среда не содержит центров или ядер кристаллизации, которые могли бы спровоцировать образование кристаллов льда. Именно поэтому вода остается в жидкой форме, даже будучи охлажденной до температуры ниже нуля градусов по Цельсию. Когда процесс кристаллизации запускается, можно наблюдать, как «сверхохлажденная» вода в одно мгновение превращается в лед. Убедитесь сами — смотрите ролик на нашем сайте.
3. «Стекловидная» вода.
Быстро, не задумываясь, скажите, сколько различных состояний есть у воды? Вы сказали, три? Твердое, жидкое, газообразное? А вот и нет. Ученые выделяют как минимум 5 состояний «жидкой» воды и 14 состояний льда. Помните разговор про сверхохлажденную воду? Так вот, что бы вы ни делали, при температуре -38 °C самая сверхохлажденная вода внезапно превратится в лед. А что же произойдет при дальнейшем понижении температуры? При -120 °C лед становится тягучим, как патока, а при -135 °C и ниже он превращается в «стеклянную» или «стекловидную» воду – твердое вещество с отсутствием кристаллов.
4. Квантовое число воды.
На молекулярном уровне воде есть чем удивить ученых. В 1995 году проводимый учеными эксперимент по рассеянию нейтронов дал неожиданный результат: было обнаружено, что нейтроны, направленные на молекулы воды, «видят» на 25% меньше протонов водорода. Оказалось, что на скорости одной аттосекунды (10 в минус 18 степени секунд) имеет место необычный квантовый эффект, и химическая формула воды из привычной Н2О превращается в Н1,5О!
Что такое одна аттосекунда, спросите вы? Это время, за которое свет проходит расстояние, сравнимое с размерами молекулы воды.
5. Есть ли у воды память?
Альтернативная официальной медицине гомеопатия утверждает, что слабый раствор лекарственного препарата может оказывать лечебный эффект на организм и сохранить свойства раствора первоначальной концентрации, даже если коэффициент разбавления настолько велик, что в растворе уже не остается ничего, кроме молекул воды. Приверженцы гомеопатии как метода лечения объясняют этот парадокс концепцией под названием «память воды». В 2002 году международная группа ученых во главе с профессором Мэдлин Эннис из Королевского университета в Белфасте, ранее критиковавшая принципы гомеопатии, заявила о том, что ей удалось доказать реальность эффекта «памяти воды» Однако опыты, проведенные под наблюдением независимых экспертов, результатов не принесли. Дискуссия о феномене «памяти воды» продолжается.
- Якщо ви думали ,що залізо — міцне і надійне, ви помиляєтеся. Залізо, нагріте до 5000 градусів Цельсія, стає газоподібним .
- Безліч хімічних елементів отримали свою назву на честь країн або інших географічних об’єктів. Відразу 4 елемента — ітрій ,ітербій , тербий і ербій — були названі на честь шведської села Іттербю, біля якої виявили велике родовище рідкоземельних металів.
- За легендою, думка про систему хімічних елементів прийшла до Менделєєва увісні, протее відомо, що одного разу на запитання, як він відкрив періодичну систему, вчений відповів: «Я над нею, може бути, двадцятьроків думав, а видумаєте: сидів і раптом … готово».
- Літій — найлегший метал. Він спливає, наприклад, в гасі.
- Водень — найпоширеніша речовина у Всесвіті (приблизно 90 % всіх атомів у всесвіті ) .
- Водень — найлегший газ. Маса 1 літраводню в газоподібному стані складає всього 0,08988 грам .
- Вода може замерзнути в трубопроводі при температурі +20 ° C ,якщо в цій воді присутній метан ( якщо бути точніше , з води і метану утворюється газовий гідрат ) . Молекули метану «розштовхують» молекули води, так як займають більший об’єм. Це призводить до зниження внутрішнього тиску води і підвищенню температури замерзання.
- У кожному літрі морської води приблизно 25 грамів солі.
- У Світовому океані в 1 т води міститься приблизно 7 мг золота. А загальна масса цього металу в водах океану становить 10 млрд. тонн .
- Найбільшим існуючим зараз платиновим самородком є « Уральськийгігант » вагою 7 кг 860,5 р. Зберігається в Алмазному фонді Московського Кремля.
- Ртуть — не єдиний метал ,який перебуває в рідкому стані при кімнатній температурі. Галій( Ga ) у руках плавиться , цезій ( Cs ) і францій (Fr) також знаходяться в рідкому стані при кімнатній температурі.
- У хімії є таке поняття — сублімація , яке позначає прямий перехід речовини з твердого в газоподібний стан, минаючи рідку фазу. У побуті найчастіше таке явище зустрічається при випаровуванні сухого льоду, який перетворюється на вуглекислий газ. _______________________________________________________________________________________________________________________________________________________________________ 1.Вода може замерзнути в трубопроводі при температурі +20 ° C, якщо в цій воді присутня метан (якщо бути точніше, з води і метану утворюється газовий гідрат). Молекули метану «розштовхують» молекули води, так як займають більший об'єм. Це призводить до зниження внутрішнього тиску води і підвищенню температури замерзання. 2. Небитке скло було винайдено випадково хіміком з Франції Едуардом Бенедиктом, який в 1903 році випадково впустив колбу з нитроцеллюлозой. Колба тріснула, але не розбилася. Після вивчення колби хімік зайнявся створенням першого лобових стекол, які стали прототипом сучасних, які допомагають зменшити кількість жертв, постраждалих в автомобільних аваріях.
-
3. Американські та англійські дослідники в 1985 році відкрили вуглецеві сполуки, які нагадували за формою футбольний м'яч. Відкриття мало отримати назву на честь футбольного м'яча, але дослідники так і не змогли домовитися яке з двох назв, футбол або сокер, використовувати і з'єднання отримали назву фулерени в честь Фуллера, архітектора, який з тетраедрів склав геодезичний купол.
4.Хто відкрив фтор Виділення чистого фтору з фторсодержащих речовин було однією з найважчих експериментальних завдань для хіміків усього світу. Фтор має виняткову здатність до реакції з іншими речовинами; причому нерідко ця реакція протікає із запалюванням і вибухом. Однією з перших жертв серед дослідників фтору стали два члени Ірландської Академії наук брати Георг і Томас Нокс. Томас загинув від отруєння фтороводень, а Георг став інвалідом. Наступним став бельгійський хімік П. Лайет. Болісну смерть при виділенні фтору прийняв французький хімік Джером Никлес. Надихавшись великою кількістю фтороводорода, отруїлися й отримали опіки різного ступеня, французькі хіміки Жозеф Гей-Люссак, Луї Тенар і англійський хімік Гемфрі Деві. При спробі отримати фтор за допомогою електролізу його сполук грунтовно підірвали своє здоров'я французький хімік Едмон Фремо і англійський електрохімік Георг Гор. І тільки в 1886 році французькому хіміку Анрі Муассану вдалося отримати фтор порівняно безпечним способом. В результаті експерименту, Муассан з'ясував, що при електролізі суміші рідкого безводного HF і гідродіфторіда калію (KHF2) в платиновому посудині на аноді виділяється світло-жовтий газ із специфічним різким запахом. Однак, при Муассан доповіді в Паризької академії наук про своє відкриття, ліве око вченого був прикритий чорною пов'язкою. Нобелівська премія з хімії була присуджена Муассану в 1906 г «в визнання великого обсягу досліджень - отримання елемента фтору і введення в лабораторну і промислову практику електричної печі, названої його ім'ям».
-
. Хто відкрив хлор Першовідкривачем хлору є фармацевт зі Швеції, Карл Шеєле, чиї досліди і відкриття в галузі хімії були справді унікальні, за словами його сучасника, французького хіміка Жана Батіста Дюма, Шеєле: »не міг доторкнутися до чого-небудь без того, щоб тут же не зробити відкриття ». Уже в 32 роки йому було прісвоіно звання члена Стокгольмської академії наук, хоча він був усього лише помошником аптекаря, тоді ж він зайняв місце керуючого аптекою, що належала вдові Маргариті Соннеман, і яка за два дні до смерті Шеєле стала його законною дружиною. Ось як описував Шеєле досвід, вироблений ним в 1774 році: «Я помістив суміш чорної магнезії з муріевой кислотою в реторту, до шийки якої приєднав міхур, позбавлений повітря, і поставив її на піщану баню. Міхур наповнився газом, забарвити його в жовтий колір: Газ мав жовто-зелений колір і пронизливий запах ». У 1812 році французький хімік Гей-Люссак присвоїв цьому газу нову назву - хлор, в перекладі з грецької «жовто-зелений». Хто відкрив бром Бром був відкритий випадково, молодим лаборантом - Антуаном-Жеромом Баларом. Балар досліджував маткові розсоли соляних боліт Франції. Під час проведення чергового досвіду, він впливав на соляний розсіл хлором, і звернув увагу на появу яскравої жовтого забарвлення, викликаної вступили в реакцію містяться в розчині броміду натрію з хлором. Через пару років інтенсивної роботи Балар зміг отримати необхідну кількість темно-бурого рідини, давши назву - муріди. В Паризької Академії наук, Французькі хіміки, Гей-Люссак і Тенар підтвердили відкриття Баларом нової речовини, але вирішили що назва не зовсім вдале і запропонували своє - «бром», в перекладі з грецької «смердючий». Його сучасник, французький хімік Шарль Жерар, який не отримав кафедру хімії у Французькому коледжі, яку передали Баларам, хоч і високо оцінив відкриття брому, але й не зміг утриматися від кілкого зауваження: «Це не Балар відкрив бром, а бром відкрив Балара!» Хто відкрив йод У 1811 році французький хімік-технолог і аптекар Бернар Куртуа відкрив йод. Існує лубопитная версія цього відкриття. У Куртуа був улюблений кіт, який під час обіду зазвичай сидів на плечі у господаря. Куртуа, під час дослідів, часто обідав у своїй лабораторії. Одного разу під час одного з таких обідів кіт, чогось налякавшись, зістрибнув на підлогу, і невдало приземлився на бутлі з реактивами, що стояли біля лабораторного столу. В одному з бутлів Куртуа приготував для досвіду суспензію золи водоростей (містить йодид натрію) в етанолі, а в іншому перебувала концентрована сірчана кислота. Бутлі розбилися і рідини змішалися. З підлоги стали підніматися клуби синьо-фіолетового пара, які тут же осідали на всіх предметах в лабороторіі у вигляді найдрібніших чорно-фіолетових кристалів з металевим блиском і їдким запахом. Так було відкрито новий хімічний елемент йод.
-
.Цікаві факти про метали. У відкритому космосі ні окислений метал злипається. Як відомо в атмосфері Землі міститься кисень, який окисляє метал. Тонкий шар окислення покриває весь шматок металу, створюючи таким чином як би захисну плівку. Зате якщо взяти 2 шматка металу в космічному вакуумі і прикласти один до одного то вони склеяться. Це відбувається тому що відсутня окислена поверхня діюча як бар'єр і атоми металу можуть вільно взаємодіяти. Якщо брати Всесвіт у цілому то це ефект цілком нормальний, а випадок на нашій планеті свого роду виключення завдяки наявності кисню. Хоча це добре, адже можна не боятися, що два металевих предмета можуть злипнутися в руках
-
огляду на це всі металеві інструменти, які використовуються космонавтами у відкритому космосі мають захисне пластикове покриття. Хоча цей ефект реальний, але це не є особливою проблемою для НАСА адже навіть якщо ви візьмете із Землі в космос вже окислений інструмент він буде мати захисну плівку і не прилипне. Найбільш поширений метал в грунті Землі - алюміній. Якщо взяти всю планету в цілому, то залізо вийде на перше місце, так як воно становить більшу частину ядра Землі. Залізо є шостим з найпоширеніших елементів у Всесвіті. В межах Землі залізо на четвертому місці. Найдорожчим металом у природі є родій, вартість якого перевалює за 175 тисяч доларів. Таким чином на другому місці платина і на третьому - золото. Єдиним металом, який може зберігати рідкий стан при кімнатній температурі є ртуть. Найвищу температуру плавлення має вольфрам, саме тому його використовують як спіралі в лампах розжарювання. Найдорожчим металом, штучно створеним людиною є каліфорній 252. Орієнтовна ціна - 6500000 $ за 1 грам. В даний момент на Землі існує не більше 5 грамів цього металу. Виробляється каліфорній 252 в потужних реакторах, не дивно, що дозволити таку розкіш можуть лише США та Росія. За рік в одному реакторі виробляється всього близько 30 мкг цього рідкісного речовини. Де ж застосовується цей понад рідкісний метал? Каліфорній 252 застосовується в медицині при лікуванні ракових захворювань; в промисловості для перевірки якості зварних швів; в приладобудуванні як індикатор; каліфорній також використовується при запуску реакторів; в геології для виявлення руху ґрунтових вод і т.п ... На цьому послужний список даної речовини не закінчені
-
У головному мозку людини за одну секунду відбувається 100 000 хімічних реакцій. У 1903 році в американському штаті Канзас з нафтової свердловини раптово забив фонтан газу. До великого здивування нафтовиків, газ виявився негорючим. Нова зустріч з ним припала на роки Першої світової війни. У німецький дирижабль, що скидає бомби на Лондон, потрапив запальний снаряд, але дирижабль не спалахнув. Повільно стікаючи газом, він відлетів геть. Секретні служби Англії переполошилися: до цього німецькі дирижаблі вибухали від попадання снарядів, так як були наповнені воднем. Експерти-хіміки згадали, що задовго до війни німецькі пароплави навіщось везли як баласт монацитовий пісок з Індії та Бразилії. Цим газом був гелій. У монацитових піску, який довгий час був головним гелійсодержащім сировиною, міститься радіоактивний елемент торій, при розпаді якого утворюється гелій, по щільності поступається тільки водню, але має перед воднем перевагу: він негорючий і хімічно інертний. Нобелівська премія з хімії була присуджена Муассану в 1906 г "в визнання великого обсягу досліджень - отримання елемента фтору і введення в лабораторну і промислову практику електричної печі, названої його ім'ям". Бром відкрив нікому не відомий учитель хімії за прізвищем Балар. Знаменитий німецький хімік Юстус Лібіх (теж працював у той час над проблемою виділення брому), дізнавшись про це, єхидно зауважив: "Не Балар відкрив бром, а бром відкрив Балара". За легендою, думка про систему хімічних елементів прийшла до Менделєєва уві сні, проте відомо, що одного разу на запитання, як він відкрив періодичну систему, вчений відповів: «Я над нею, може бути, двадцять років думав, а ви думаєте: сидів і раптом ... готово ». У деяких штатах американці додають в газ, що йде по газопроводах, хімічна речовина із запахом тухлого м'яса. Це дозволяє легко знаходити місце витоку, над яким починають кружляти грифи. Хлорид кобальту можна успішно використовувати для тайнопису: літери, написані його розчином, що містить в 25 мл води 1 г солі, абсолютно невидимі і проявляються, роблячись синіми, при легкому нагріванні паперу. Німецька фірма BASF, в недалекому минулому відома багатьом меломанам, як виробник дуже якісних магнітних стрічок, насправді є великим хімічним концерном. А починалося все з виробництва таких нехитрих речей, як сода і вапно. Абревіатура BASF німецькою позначає "майстерні з виробництва соди та вапна" Водень - найпоширеніше речовина у Всесвіті (приблизно 90% всіх атомів у всесвіті). Канарки дуже чутливі до вмісту в повітрі метану. Цю особливість використовували свого часу шахтарі, які, спускаючись під землю, брали з собою клітку з канаркою. Якщо співу давно не було чути, значить слід підніматися нагору якомога швидше. В Антарктиді з льодовика Тейлора часом виходить Кривавий водоспад. Вода в ньому містить двовалентне залізо, яке, з'єднуючись з атмосферним повітрям, окислюється і утворює іржу. Це й надає водоспаду криваво-рудий колір. Однак двовалентне залізо у воді виникає не просто так - його виробляють бактерії, що живуть в ізольованому від зовнішнього світу водоймі глибоко під льодом. Ці бактерії зуміли організувати життєвий цикл при повній відсутності сонячного світла і кисню. Вони переробляють залишки органіки, а «дихають» тривалентним залізом з навколишніх порід. У 1669 році німецький алхімік Бранд Хенниг в пошуках філософського каменя вирішив спробувати синтезувати золото з людської се







