Тема уроку. Сульфатна кислота. Фізичні й хімічні властивості
Тема: вивчити фізичні й хімічні властивості сульфатної кислоти; ознайомити учнів зі специфічними властивостями концентрованої сульфатної кислоти; показати значення сульфатної кислоти.
Тип уроку: комбінований урок засвоєння знань, умінь і навичок і творчого застосування їх на практиці.
Методи та прийоми: навчальна лекція, фронтальна робота з опорною схемою, демонстраційний експеримент, демонстрація презентації.
Обладнання: періодична система хімічних елементів, таблиця розчинності, ряд активності металів, презентація "Сульфатна кислота".
Демонстрація 6. Хімічні властивості розведеного розчину сульфатної кислоти.
Демонстрація 7. Взаємодія концентрованої сульфатної кислоти з міддю.
II. Актуалізація опорних знань
1. Аналіз практичної роботи 1, обговорення типових помилок, коригування знань
2. Робота біля дошки за питаннями
1) Установіть відповідність.
N2O5 H2СO3
SO2 HN03
СO2 H2SO4
SO3 H2SO3
2) Запишіть рівняння гідратації оксидів із завдання 1.
3) Здійсніть перетворення.
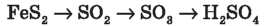
4) Обчисліть масу сульфатної кислоти, яку можна одержати з 1 т піриту, що містить 10 % домішок, якщо вихід продукту реакції становить 87 %.
III. Вивчення нового матеріалу
1. Фізичні властивості сульфатної кислоти Розповідь учителя.
2. Демонстрація 6. Хімічні властивості розчину сульфатної кислоти
1) Сильний електроліт, у розчині практично повністю дисоціює на йони:
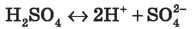
2) Утворює два ряди солей: кислі й середні. Які саме з них утворяться, залежить від кількісного співвідношення реагентів:
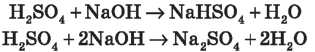
(демонстрація 2, учні біля дошки складають йонно-молекулярні рівняння) 3) 3 основними оксидами:
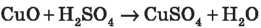
(демонстрація зі складанням йонних рівнянь реакцій)
4) Може витісняти більш слабкі кислоти в процесі взаємодії з їхніми солями:

5)3 металами розведена й концентрована кислоти взаємодіють по-різному. Розведена реагує з металами до Н:
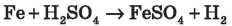
(демонстрація зі складанням йонних-молекулярних рівнянь)
3. Специфічні властивості концентрованої сульфатної кислоти
1) Обвуглювання органічних речовин, що складаються з Карбону й Гідрогену. Якщо цукор змішати з концентрованою H2SO4, маса чорніє й розігрівається й незабаром зі стаканчика починає виповзати пориста чорна маса (за технічної можливості демонструємо дію концентрованої сульфатної кислоти на цукор):
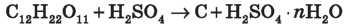
2) Концентрована H2S04 за кімнатної температури не взаємодіє з деякими металами. Це дозволяє перевозити кислоту (≥ 75 %) у сталевих цистернах.
3) Унаслідок нагрівання діє майже на всі метали до Ag включно (крім Pt, Au та деяких інших). У цьому випадку водень не виділяється, а утворюються продукти відновлення S+6: SO2, H2S, S, а також сіль і вода. Продукти залежать від активності металу й умов реакції. Умовно можна прийняти, що сульфатна кислота відновлюється:
• з малоактивними металами — до SO2:
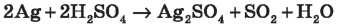
• у результаті взаємодії з більш активними металами можуть виділятися S02, H2S і S. Наприклад, узаємодія з Zn (залежно від умов — температури й концентрації):

Демонстрація 7. Взаємодія концентрованої сульфатної кислоти з міддю
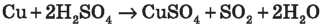
4. Значення сульфатної кислоти й сульфатів у народному господарстві
Повідомлення учнів. Демонстрація презентації
Застосування H2SO4
Фундамент хімічної промисловості.
Виробництво мінеральних добрив.
Очищення поверхні металів перед нанесенням металевих покриттів.
В акумуляторах.
IV. Первинне застосування отриманих знань
Завдання 1. Як концентрована H2SO4 діятиме на індикатори? Відповідь обґрунтуйте.
Завдання 2. Напишіть рівняння реакцій узаємодії концентрованої сульфатної кислоти з натрієм, цинком, алюмінієм, вуглецем у молекулярній формі й розставте коефіцієнти методом електронного балансу (самостійна робота зі взаємоперевіркою):
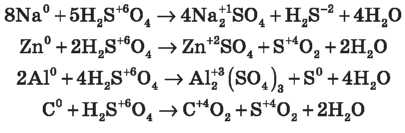
Чому розрізняються хімічні властивості розведеної та концентрованої сульфатних кислот?
У цистернах з яких металів можна транспортувати концентровану сульфатну кислоту? (Назвіть умови.)
Чому ці самі цистерни не можна використовувати для перевезення розчинів сульфатної кислоти?
Опрацювати матеріал параграфа, відповісти на запитання до нього, виконати вправи.
Творче завдання: підготувати повідомлення (презентації) про сульфати та їх застосування.







